生活被装点的五彩斑斓,每一处景色都交织着人们的回忆,然而在一些人眼中,这缤纷的世界却正在慢慢变得苍白。
夜里的村子并不宁静,大家都在举着手电四处奔走,寻找一个走失的老太太。一宿的忙碌在天亮时终于有了回报,老太太的大儿子领着满头露水的老母亲走进自家院子。老太太看见进院的大海棠树,咧了嘴笑出了声,说到家了,到家了,然后嬉笑着坐在树下面,哼着她姑娘时候唱的调子。这是我对阿尔茨海默病最早的印象,那时候年龄太小,只记得老太太的曲调里,混杂着几道子女们蜿蜒的哭声。我们时常听到有人说谁家的老人糊涂了,找不着家,打人,偷抢别人的东西,连自己亲儿子都认不出来了,这可能就是患了阿尔茨海默症。
阿尔茨海默病直接对患者的记忆产生进行性的损害,进一步影响患者的思想以及行为,对病人生活质量产生严重的影响。而随着病情的一步步加深,照顾病人的患者家属所产生的与患者无法沟通和病情治疗无望的情绪,将是击溃他们的最后一根稻草。有研究显示,与配偶未患有阿尔茨海默病的人相比,那些照顾阿尔茨海默病的老年人,患抑郁症的概率会增加30% 1。
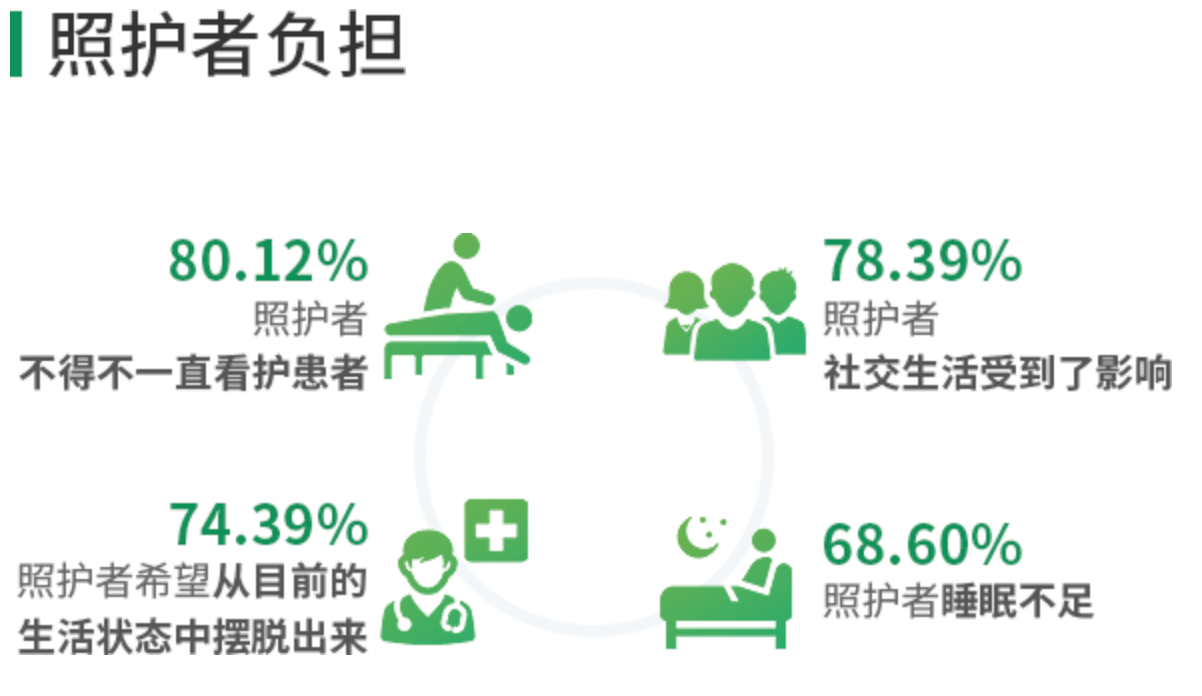
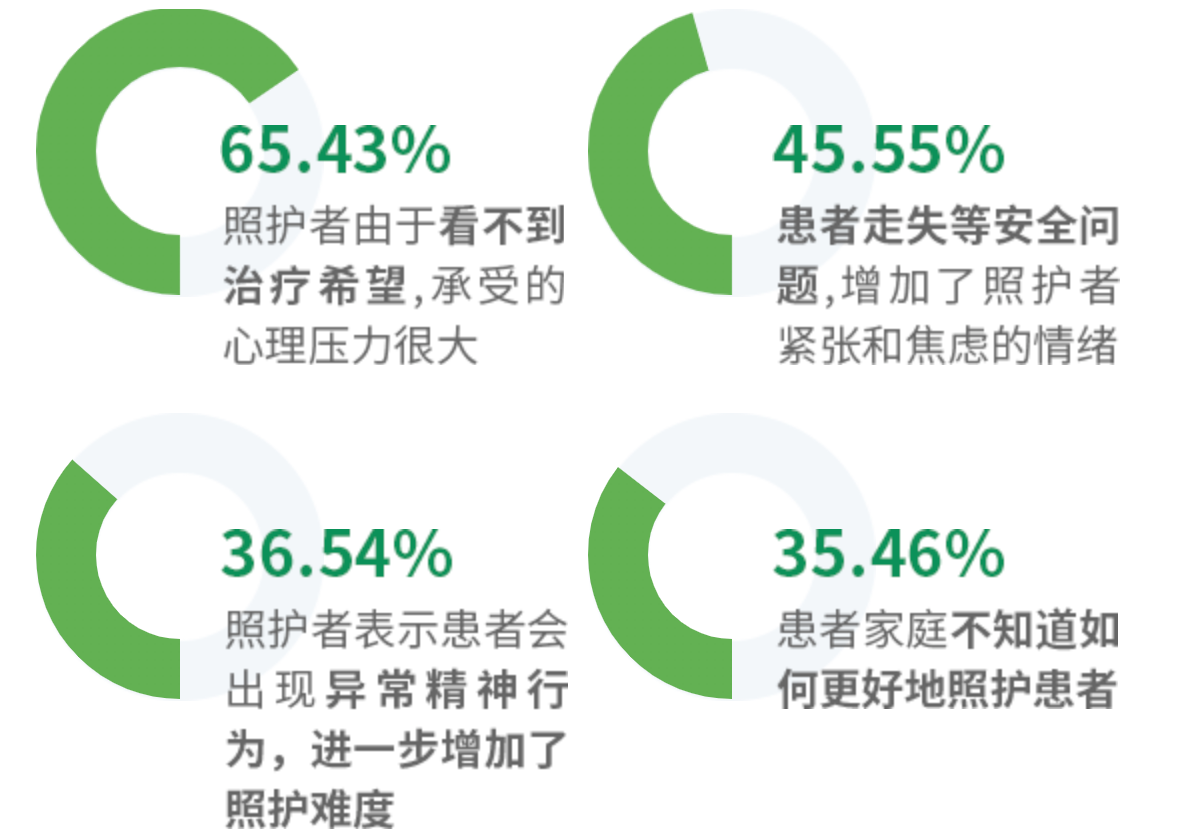
图源:2019中国阿尔茨海默病患者家庭生存状况调研报告
我国阿尔茨海默症现状
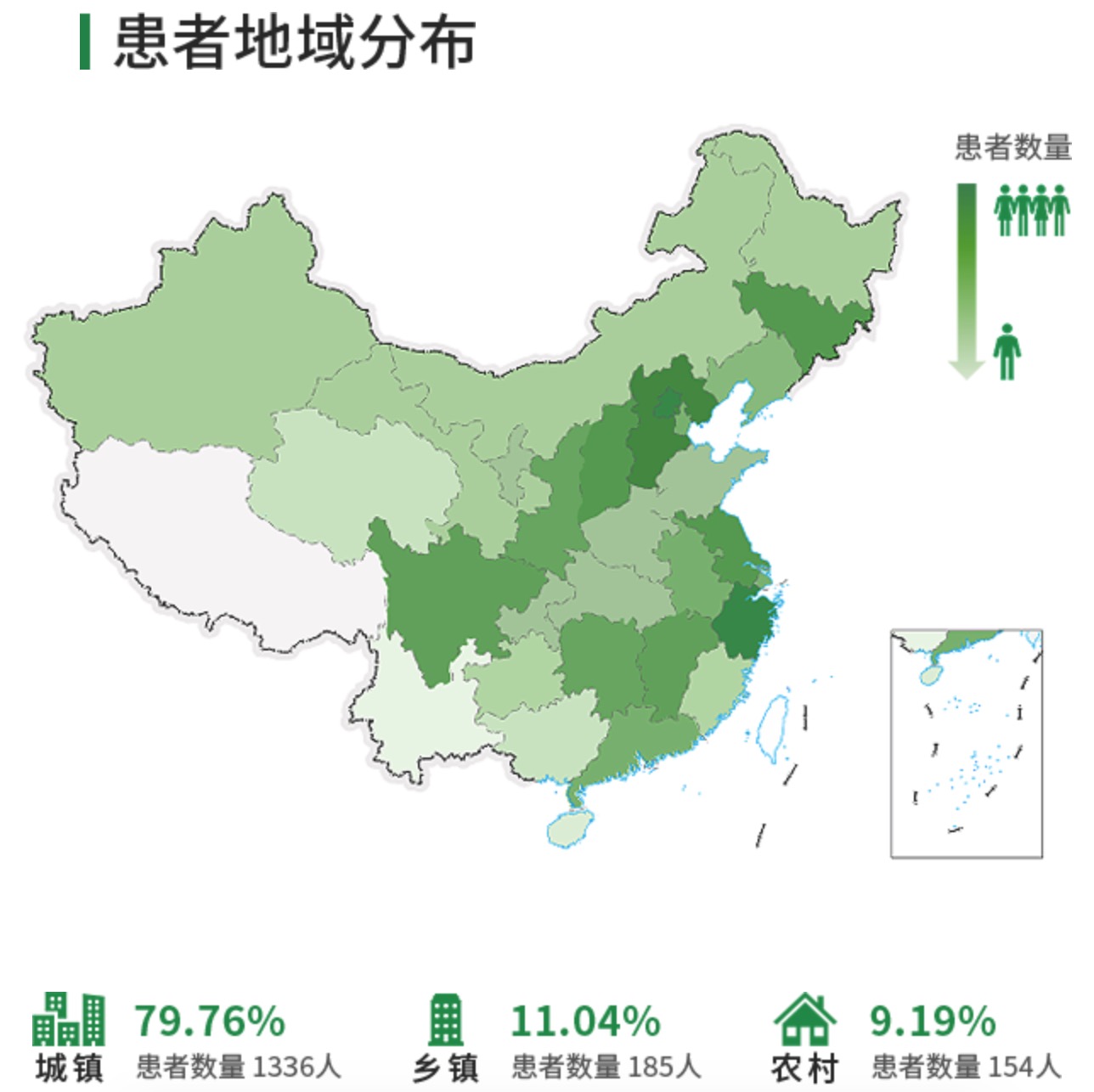
图源:2019中国阿尔茨海默病患者家庭生存状况调研报告
随着中国人口老龄化日益加剧,据2016年世界卫生组织发布的《中国老龄化与健康国家评估报告》估计,到2040年,中国60岁及以上人口的比例将从2010年的12.4%上升至28% 。随着人口的老年化,老年人的相关问题已直接关系到国民经济发展和社会稳定。阿尔茨海默病(AD)是一个日益严重的公共卫生问题,影响着全球数百万患者,每年造成数十亿美元的损失。预计到2050年,AD痴呆症将对全球人口产生破坏性影响,受影响的人数将达到1.31亿2。2020年1月发布的《2019中国阿尔茨海默病患者家庭生存状况调研报告》显示,截至2019年中国有1000多万阿尔茨海默病患者,是世界上患者最多的国家,约占世界痴呆总人口的25%。随着老龄化社会的来临,预计到2050年我国阿尔茨海默症患者将超过3000万。然而这种疾病却并没有得到应有的重视。在中国,阿尔茨海默病有三个“低”:认知程度低,就诊率低以及接受治疗比例低。目前该病无法治愈,只能通过正确的措施,改善和延缓病情。早诊断、早干预、早治疗是预防改善该病的主要手段。
阿尔茨海默症的致病机制
神经性纤维缠结与老年斑是AD的两个基本病理特征3。而老年斑的主要成分Aβ蛋白是由β淀粉样斑原始蛋白(APP)经过β分泌酶(β-secretase)、γ分泌酶(γ-secretase)连续切割成的大小在38-43之间的小肽形成的4、5。较长一点肽段如Aβ42,Aβ43普遍被认为比短一点Aβ40更容易聚合形成老年斑6。在产生Aβ42过程中,APP首先被β-secretase 1(BACE1)切断开来生成位于胞外的N端sAPPβ与C端的C99蛋白。C99蛋白再被γ-secretase (PSEN1,PSEN2,NCT和APH-1四个亚基组成)近一步切成片段Aβ42或者Aβ40与CTFγ。Aβ42在胞外比Aβ40更容易聚集形成老年斑7。家族性的老年痴呆症(FAD)主要由APP基因和PSEN1(γ-secretase 催化亚基)显性遗传主导。临床试验中γ-secretase的抑制剂在临床上对AD未显示治疗效果,所以PSEN1错义突变切割C99导致的Aβ42与Aβ40比值上升是AD的主要原因8。AD的另外一个致病机制NFT,是Tau蛋白磷酸化后与正常Tau蛋白聚集形成。关于阿尔茨海默症的具体致病机制现在认不清楚,其致病机制假说很多,包括氧化应激假说、基因突变假说、胰岛素假说、血管因素假说、Aβ-淀粉样肽级联假说以及Tau 假说等。其中大部分实验数据都支持Aβ-淀粉样肽级联假说9、10。Aβ-淀粉样肽级联假说认为人体中存在着Aβ生成和降解的动态平衡机制,而AD早期患者脑中Aβ42升高聚集形成老年斑,导致Tau蛋白磷酸化形成NFT,神经元死亡、记忆力衰退、行为能力丧失和最终死亡。
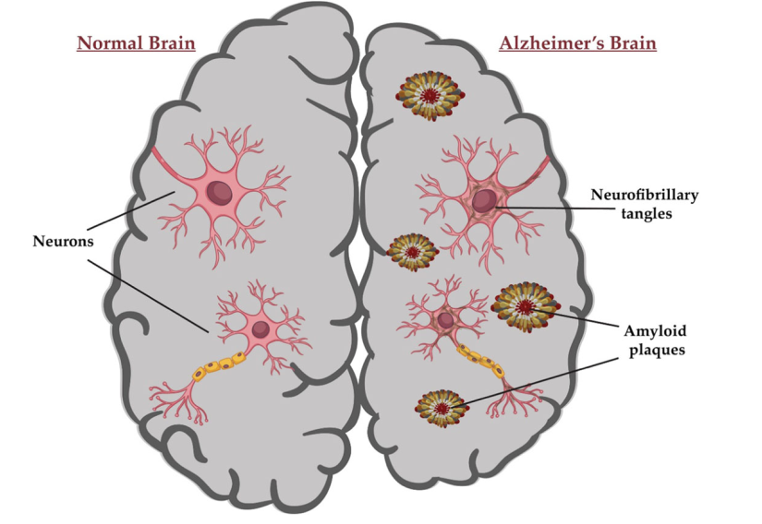
图源:BACE1 inhibitors: Current status and future directions in treating Alzheimer’s disease
研究治疗从未停止
在中国老年保健协会阿尔茨海默病分会(ADC)、人民日报社《健康时报》共同发起的公益调研结果显示,每一个数字背后都是一个沉重的家庭负担,阿尔茨海默病防治的药物研究已经刻不容缓。
自 1906 年首次报告 1 例 51 岁女性病例以来,AD 载入医学史册已近 110 年,但迄今尚无有效的药物来预防、改善或逆转 AD 的发生。因此研发新型、有效的 AD 治疗药物成为全球关注的热点。2019年有139种药物在进行临床试验,然而截止到2020年2月27日,只有121种药物正在进行阿尔茨海默病的临床实验,自2004年以来,FDA已经16年没有批准新药2、11。尽管如此,对于阿尔茨海默病致病机理的研究以及治疗药物基础研究从未停止过。
三启生物一直致力于神经中枢疾病的研究,基于β淀粉样斑致病方向,我们利用基因编辑工具,建立了人诱导多能干细胞与阿尔茨海默病致病基因的高效、稳定的新型阿尔茨海默疾病细胞模型,该模型通过验证确认可以在体外高表达Aβ42,同时满足稳定批量化细胞生产的要求。我们相信,通过这个细胞模型,可以便捷地研究阿尔茨海默症的致病机理和开发针对该病的新型药物。
更多关于我们的AD/PD药筛平台的最新进展和数据,可以关注我们在2020年10月12-16号的ThermoFisher 5 Days of Stem Cells Virtual Event:
Jiayin Yang: iPSC-based high throughput platforms for screening novel therapeutics for treatment of Alzheimer’s disease and Parkinson’s disease
文作者:江利香,闫玉波
图片已标注出处,如有侵权请联系删除
三启生物神经细胞相关产品
| 货号# | 名称 |
| iN-300 | 神经干细胞 |
| iN-301 | 混合神经元细胞 |
| iNM-001 | 神经干细胞扩增培养基 |
| iNM-002 | 神经元保护剂筛选试剂盒 |
| iNM-003 | Aβ42抑制剂筛选试剂盒 |
| iNM-004 | 神经细胞毒性测试试剂盒 (基于CCK8检测,包括NPC,培养基及阳性对照) |
| iNM-005 | Ready to use 96孔板混合神经元 |
| iNM-006 | 神经元活性测试试剂盒 |
| iNM-007 | 神经元成熟培养基 |
参考文献:
【1】Melissa Harris, Depression Can Deepen Over Time for Alzheimer’s Caregivers. Medicine Net. 2020.9.9;
【2】Jeffrey Cummings, Garam Lee, Aaron Ritter, et, al. Alzheimer’s disease drug development pipeline: 2020. [J]. Alzheimers Dement (N Y) .2020:6;
【3】Estus S, Golde TE, Kunishita T, Blades D, Lowery D, Eisen M, Usiak M, Qu XM, Tabira T, Greenberg BD and et al. Potentially amyloidogenic, carboxyl-terminal derivatives of the amyloid protein precursor. Science. 1992;255:726-8.
【4】Golde TE, Estus S, Younkin LH, Selkoe DJ and Younkin SG. Processing of the amyloid protein precursor to potentially amyloidogenic derivatives. Science. 1992;255:728-30.
【5】Suzuki N, Cheung TT, Cai XD, Odaka A, Otvos L, Jr., Eckman C, Golde TE and Younkin SG. An increased percentage of long amyloid beta protein secreted by familial amyloid beta protein precursor (beta APP717) mutants. Science. 1994;264:1336-40.
【6】Zhang X and Song W. The role of APP and BACE1 trafficking in APP processing and amyloid-beta generation. Alzheimers Res Ther. 2013;5:46.
【7】Doody RS, Raman R, Farlow M, Iwatsubo T, Vellas B, Joffe S, Kieburtz K, He F, Sun X, Thomas RG, Aisen PS, Alzheimer’s Disease Cooperative Study Steering C, Siemers E, Sethuraman G, Mohs R and Semagacestat Study G. A phase 3 trial of semagacestat for treatment of Alzheimer’s disease. N Engl J Med. 2013;369:341-50.
【8】Pike CJ, Burdick D, Walencewicz AJ, Glabe CG and Cotman CW. Neurodegeneration induced by beta-amyloid peptides in vitro: the role of peptide assembly state. J Neurosci. 1993;13:1676-87.
【9】Gschwind M and Huber G. Apoptotic cell death induced by beta-amyloid 1-42 peptide is cell type dependent. J Neurochem. 1995;65:292-300.
【10】Hardy JA and Higgins GA. Alzheimer’s disease: the amyloid cascade hypothesis. Science. 1992;256:184-5.
【11】 Jeffrey Cummings, Garam Lee, Aaron Ritter, et, al. Alzheimer’s disease drug development pipeline: 2019. [J]. Alzheimers Dement (N Y) .2019:5




